Взаимодействие загрязняющих веществ с озоном происходит за счет прямой реакции с молекулами озона или же с радикалами, появляющимися в процессе его распада. Более активно озон взаимодействует с анионами, чем с нейтральными и катионными веществами.
Озон, являясь активным окислителем, взаимодействует со многими органическими и неорганическими веществами. Из галогенов с озоном не реагирует фтор и практически не вступает во взаимодействие хлор. Бром окисляется озоном сначала до гипобромита, а затем и до броматных соединений. При этом образующийся бромид может параллельно взаимодействовать с веществами органического происхождения и аммиаком. Йод окисляется озоном очень быстро с образованием йодатов и йодноватистой кислоты. Соли галогеносодержащих кислот уже не поддаются озоновому окислению. Практически нейтральными к озону являются азот и его соединения, в том числе аммиак и ионы аммония, а так же нитраты, за исключением аминов, хорошо взаимодействующих с гидроксильными радикалами. Токсичные цианиды легко окисляются озоном в цианаты, дальнейшее окисление которых происходит очень медленно и ускоряется только в присутствии ионов меди, замедляясь при наличии в растворе ионов железа. Сера и сульфитные при взаимодействии с озоном окисляются до сульфатов. Что же касается реакций с металлами, то озон достаточно активно окисляет железо и марганец, кобальт и никель, образуя оксиды и гидроксиды, удаляемые из раствора при флокуляции или фильтрации. Практически пассивен в отношении озона хром, хотя при определенных условиях он может быть окислен им до максимальной степени окисления, шестивалентного хрома.
1.1 Введение
Озон был открыт в 1840 г. швейцарским химиком Христианом Шомбайном, после экспериментов по электролизу кислот. Очень скоро, в результате ряда исследований было показано, что озон – это трехатомный кислород, газ при стандартных условиях, характерными свойствами которого является его способность к окислению многих веществ и дезинфекция микрофлоры. Эти свойства очень скоро были использованы в промышленности для обработки питьевой воды. В самом конце 90х XIX столетия в Нидерландах и Германии делались попытки дезинфицировать воду для питья с помощью озона. Общепризнанной датой рождения озонной технологии водоподготовки принято считать 1906 г., когда во французском городе Ницца начала работать станция водоподготовки, носившая символическое название «Добрый путь» («bon voyage») с производительностью по воде 22,5 м³/сутки. Станция успешно работала до 1970 г., когда была модернизирована. Эта практика получила в дальнейшем широкое распространение, о чем свидетельствуют следующие данные: В Германии количество предприятий, использующих озон выросло в период с 1984 по 2000г. С 30 до 300, а в США с 1954 по 1997 с 10 до 5500 соответственно.
В России эффективность озонирования для водоподготовки была оценена практически в то же время, что и за рубежом. В 1901 г. 5-ый водопроводный съезд заслушал доклад инженера Н.П. Зимина по озонированию воды; последний характеризовал «озонирование воды, как средство по устранению недостатков ее фильтрования при городских водопроводах».
В 1905 г. при Петропавловской больнице в Санкт-Петербурге была введена строй экспериментальная установка по озонированию воды. Было установлено, что число бактерий снижалось в среднем на 98,8%, улучшался вкус и отсутствовал цвет очищенной воды. В 1911 г. в Санкт-Петербурге начала работать самая крупная в мире в то время станция озонирования воды. При открытии, ее производительность составляла 44,5 тыс. м³/сутки обработанной воды.
Обзор представлений об озоне, его получении и применении в различных областях в начале ХХ века дан в книге русского инженера В.В. Караффа-Корбутта «Озон и его применение в промышленности и санитарии», вышедшей в 1912 г.
Одной из первых советских монографий на эту тему является книга В.Ф. Кожинова и И.В. Кожинова «Озонирование воды». Эти работы относятся к прошлому веку. За последнее время в производстве озона был достигнут значительный прогресс, при этом открылись новые весьма перспективные области использования озона.
1.2 Озон, его свойства и основные реакции с различными веществами.
1.2.1 Физико-химические свойства озона.
При нормальных условиях озон – газообразное бесцветное вещество, обладающее резким запахом. Считается, что запах озона – это запах свежего воздуха после грозы. Это действительно так, но лишь в том случае, если его концентрация очень мала и составляет доли предельно допустимых концентраций (ПДК). Детальное описание физико-химических свойств озона рассматривается в многочисленных работах, в частности . Некоторые основные физико-химические свойства озона приведены в таблице 1.1 .
Таблица 1.1 .Основные физико-химические свойства озона.
Чистый озон взрывоопасен. Он не обладает стабильностью и быстро разлагается. На разложение озона влияет множество факторов: температура, рН, присутствие веществ, подлежащих окислению, и пр.
1.2.2 Растворимость озона в воде
При растворении озона в воде, его концентрация постепенно повышается и достигает предельных значений для данных условий.
Растворимость озона в воде может быть выражена либо в виде так называемого коэффициента Бунзеа – β, показывающего отношение объема растворенного озона, приведенного к нормальным условиям, к объему воды (Vоз/Vв), либо в абсолютных значениях растворенного озона (г/л). При этом считается, что процесс растворения подчиняется закону Генри, согласно которому количество растворенного озона пропорционально давлению газообразного озона над раствором. Этот закон может быть записан в виде:
C стац = β
C стац - растворимость озона, г/л;
β – коэффициент Бунзена;
M – плотность озона = 2,14 г/л;
Pγ – парциальное давление озона в рассматриваемой газовой среде.
Следует отметить, что растворимость озона гораздо выше основных атмосферных газов – азота и кислорода, но слабее таких окислителей, как хлор и двуокись хлора. Растворимость озона повышается с понижением температуры воды. При этом наблюдается большой разброс в экспериментальных данных различных авторов, представленных в таблице 1.2 .
Таблица 1.2 Растворимость озона в воде.
|
Т, °С |
По данным |
По данным |
По данным |
||||
|
Β (л О3/л Н2О) |
Растворимость, г/л |
Β (л О3/л Н2О) |
Растворимость, г/л |
Β (л О3/л Н2О) |
Растворимость, г/л |
||
1.2.3 Разложение озона в воде
Одновременно с растворением озона в воде происходит его разложение. При этом скорость его распада, как и обратная величина «время жизни» зависит от температуры воды и, в основном, от состава воды. В первую очередь от наличия в воде различных примесей, особенно некоторых органических соединений и ионов металлов.
Время жизни в однократнодистеллированной воде 20 минут, а в обычной воде несколько минут.
1.3 Реакции озона с неорганическими веществами.
Озон может реагировать с различными, находящимися в воде веществами по двум различным механизмам – непосредственно как озон (в молекулярной форме) и виде радикала ОН*, который возникает при распаде озона в воде. Считается, что в нейтральной воде эти 2 канала реакций распределены поровну. В кислой среде преобладает молекулярный механизм, а в щелочной – радикальный.
Поскольку озон выступает в химических реакциях как окислитель, то можно судить о его окислительной способности, по так называемой величине окислительного потенциала. Значение величин окислительных потенциалов различных веществ –окислителей приведены в таблице 1.3 .
Таблица 1.3. Окислительно-восстановительные потенциалы различных веществ.
Из таблицы 1.3. следует, что озон является очень сильным окислителем. Из стабильных веществ он уступает только фтору и превосходит хлор в полтора раза .
1.3.1 Реакция озона с металлами.
Являясь сильным окислителем, озон в газовой фазе окисляет большинство металлов за исключением золота и некоторых металлов платиновой группы, оксиды высших степеней окисления, но эти реакции требуют обычно присутствие следов влаги. Щелочные и щелочноземельные металлы окисляются озоном так же, как и кислородом, только с большей скоростью. Интересно, что пластинки золота и платины (и в меньшей степени серебра и меди) в атмосфере сухого озона приобретают отрицательный электрический заряд.
Металлическое серебро хорошо окисляется озоном, как во влажном, так и в сухом газе в интервале температур от комнатной до 1000С с образованием коричневого оксида Ag2O. Последний является хорошим катализатором разложения озона.
Металлическая ртуть, как и серебро, окисляются озоном уже при комнатной температуре, при этом поверхность теряет уже присущую ей подвижность, прилипает к стеклу, а мениск ртути становится более плоским. Расплавленное олово при 5000С в присутствии 1% озона покрывается оксидной пленкой . Озон в присутствии воды окисляет свинец с образованием гидрооксида. В отсутствие влаги основным продуктом этой реакции является темно-коричневый диоксид свинца.. Полирование поверхности меди, цинка, железа, различных сталей в атмосфере влажного озона покрываются рыхлыми окислыми пленками, как и при обычной атмосферной коррозии. В сухой атмосфере эти поверхности пассивируются озоном, образуя защитные пленки. Аналогичная картина наблюдается для меди и цинка.
Взаимодействие металлов с озоном в растворах протекает более разнообразно. Так, если на золото озон в газовой фазе не действует, то небольшие его добавки способствуют растворению золота в растворах цианистого калия в 1.5-2 раза и серебра в 3 раза.
Сильные окислительные свойства озона предложено использовать для селективного окисления минералов в водной среде. Так были получены сульфаты бария и стронция. Сульфиды тяжелых металлов являются ценным металлургическим сырьем, поэтому перевод их в водорастворимые сульфаты (или оксиды), очень давно привлекал внимание. В настоящее время по этому вопросу накоплен большой лабораторный или полупромышленный массив экспериментальных данных. Речь идет о создании на основе выщелачивания металлов озоном из кислых пульп сульфидов. Эта гидрометаллургическая технология имеет целый ряд преимуществ перед используемой в настоящее время пирометаллургией..
1.3.2 Реакции озона с неметаллами.
Неметаллы реагируют с озоном различным образом. Сухой фосфор, как белый, так и красный, окисляется озоном до P2О5. Мышьяк подобно фосфору, сере, селену, теллуру в сухой атмосфере окисляется до оксидов, а в присутствии воды образуются соответствующие кислоты, а в щелочной воде – соли.
Азот не реагирует с озоном, но окислы азота (некоторые из них) реагируют очень легко, что делает возможность устранять их из газовых выбросов целого ряда предприятий . Второй неприятный ингредиент многих газовых выбросов, двуокись серы – не реагирует с озоном в газовой фазе, но реагирует в растворе . Цианиды (цианид-ионы) легко реагируют с озоном в водном растворе, и эти процессы, а также устранение из воды железа и марганца подробно рассматриваются ниже.
Озон окисляет все галогены, кроме фтора, причем с увеличением порядкового номера элемента легкость окисления увеличивается. Эти процессы кратко рассматриваются в разделе, посвященном обработке воды в плавательных бассейнах.
1.4. Реакции озона с органическими соединениями.
Дать характеристику реакций всех основных органических веществ с озоном достаточно трудно. Возможно, лишь отметить некоторые общие положения, рассматривая прямое воздействие озона.
Насыщенные алкильные соединения реагируют с озоном очень медленно. Большинство хлорированных углеводородов и даже ненасыщенные углеводороды не реагируют прямо с озоном. В этом случае необходимо косвенное взаимодействие с озоном через радикал ОН*. Бензол окисляется озоном очень медленно, а полициклические углеводороды быстрее. Время реакции озона с фенольными соединениями составляет насколько секунд.
Карбоксильные кислоты, кетовые кислоты и ряд подобных соединений представляют собой конечные стабильные продукты процесса окисления органических веществ озоном.
Амины при нейтральных значениях рН реагируют весьма медленно с озоном, при рН › 8 реакции окисления проходят быстрее. Однако в основном реакции окисления аминов идут через ОН радикалы. Четвертичные амины (ароматические амины) реагируют с озоном быстрее.
Спирты могут взаимодействовать с озоном, образуя в качестве промежуточных соединений гидропероксиды. При этом они окисляются до карбоксильных кислот, в то время как вторичные спирты – до кетонов. Карбоновые кислоты с озоном реагируют слабо или не реагируют вообще.
Меркаптаны окисляются с озоном до сульфоновых кислот. Бисульфиты и сульфоновые соединения являются промежуточными веществами. Аминокислоты, в состав которых входит сера (цистеин, цестин и метионин) реагируют быстро.
Аминокислоты (составляющая часть белков) реагируют по электрофильному механизму.
Среди пестицидов, содержащих эфиры фосфорной кислоты, наиболее известным является паратион. Озонирование этого соединения приводит к появлению параоксона, который более токсичен, чем паратион. Дальнейшее озонирование превращает параоксон в менее токсичные вещества (например, в нитрофенол, который затем окисляется до конечных продуктов – нитратов и СО2).
1.5. Озон, как инактиватор микрофлоры.
Как уже упоминалось выше озон обладает мощным бактерицидным и вирулентным (инактивирующим вирусы) действием.
В научной литературе (особенно популярной) часто утверждается, что озон действительно дезактивирует бактерии и вирусы сильнее, чем хлор (и это будет проиллюстрировано ниже), но к количественным оценкам этого преимущества надо относится с определенными оговорками.
В настоящее время при оценке эффективности того или иного дезинфектанта используется так называемый СхТ критерий, т.е. произведение концентрации реагента на время действия.
Можно сказать, что:
ВОЗДЕЙСТВИЕ (ИНАКТИВАЦИЯ) = Концентрация * Время воздействия.
В таблице 2.1. представлены для сравнения значения СхТ критерии для различных микроорганизмов – дезинфицирующих агентов.
Таблица 2.1. Значение СхТ критерия для различных микроорганизмов (99% инактивации при 5-25 °С. СхТ критерий (Мг/л*мин)
Очевидно, что озон превосходит такие дезинфектанты как хлор, хлорамин и двуокись хлора, но по-разному для различных патогенов. Для такого патогенна как кишечная палочка (Е-coli) озон более эффективен, чем хлор, но ненамного. В то же время для криптоспоридиума отношение СхТ критериев этих дезинфекторов приближается к 1000. В принципе озону могут составить конкуренцию такие дезинфицирующие реагенты как хлор, бром, йод, двуокись хлора и серебро.
Молекулярный газообразный хлор, растворяясь в воде, распадается, производя хлористую кислоту HOCl, которая, в свою очередь, диссоциирует в воде на анион СlО- и катион Н+. Степень этой диссоциации определяется кислотностью среды. Установлено, что при рН = 8 концентрация недиссоциироавшей кислоты ≈ 20%, а при рН = 7, концентрация НСlО≈80%. Так как сильным бактерицидным действием обладает именно НСlО, то при использовании хлора (даже в виде гипохлорита) необходимо поддерживать оптимальное значение рН.
Йод, как дезинфектант, используется для инактивации микрофлоры в небольших системах водоподготовки и иногда в плавательных бассейнах небольшого объема. По своим дезинцифицирующим свойствам йод слабее хлора и тем более озона, но он более удобен в транспортировке.
Бром, в принципе, может использовать для целей дезинцификации, однако, в присутствии других окислителей он образует броматы, производные кислоты HBrO3, которые являются весьма вредными и им соответствует низкое значение ПДК. Эта проблема – образование броматов при озонировании бром-содержащих вод является достаточно серьезной, и мы остановимся на ней в разделе «Использовании озона для подготовки питьевой воды». Серебро – экзотический, но весьма слабый дезинфектант, и используется редко.
Кроме того, в последнее время отечественная и зарубежная промышленность предлагает ряд органических веществ, обладающих сильным дезинфицирующим действием. Однако все они имеют те или иные недостатки и большого распространении до настоящего времени не нашли.
Таким образом, реальным конкурентом озону может быть только хлор. К сожалению, у хлора есть существенные недостатки:
Долгое время использовался жидкий хлор из баллонов под давлением, что являлось большой проблемой с точки зрения безопасности. В настоящее время хлор получают или используют гипохлорит, который, растворяясь в воде, создает необходимую концентрацию свободного хлора. Надо отметить, что под термином «свободный хлор» понимают концентрацию хлорноватистой кислоты HСlO. Использование гипохлорита вызывают необходимость в хранении запаса реагента, но гипохлорит при хранении разлагается, и содержание свободного хлора падает.
Одно из основных неприятных свойств хлора, заключается в том, что при его реакциях с большинством органических соединений возникает целый спектр хлорорганических производных, большинство из которых сильно ядовиты. Хлорфенолы и особенно полихлорфенолы, некоторые из последних, так называемые диоксины, являются одними из сильнейших известных в настоящее врем органических ядов, причем действие этих токсинов заключается в разрушении иммунной системы человека, так что говоря о диоксинах иногда используют термин «химический СПИД».
Хлор очень легко взаимодействует с аммиаком, образуя хлорамины. Эти вещества обладают весьма слабым дезинфицирующим действием, но чрезвычайно сильно раздражают слизистые оболочки глаз и носоглотки. Хлорамины часто называют «связанным хлором». Этот связанный хлор в 5-10 раз более сильный раздражитель, чем свободный хлор.
Озон также может образовывать промежуточные соединения (by products) при озонировании газовых и конденсированных сред. Теоретически можно допустить, что образующиеся by products более токсичны, чем озон.
Эта проблема была предметом исследований многих ученых всего мира. Концентрации и состав промежуточных веществ, возникающих при озонировании, сильно зависят от того, озонируется ли питьевая или сточная вода. Безусловно, в первом случае образуется гораздо меньше by products и состав их более очевиден. Все эти вопросы будут рассмотрены в соответствующих разделах обзора. Можно резюмировать достаточно согласующиеся результаты многолетних исследований следующим образом :
В подавляющем большинстве случае промежуточные продукты окисления загрязнителей озоном МЕНЕЕ ТОКСИЧНЫ, чем исходные ингредиенты.
Прямое сопоставление промежуточных веществ, образующихся при сравнительных экспериментах по хлорированию и озонированию показало, что в первом случае образуется гораздо больше нежелательных by products .
Прямое сопоставление хлора и озона в качестве дезинфектантов микрофлоры делалось в многочисленных экспериментальных исследованиях и на работающих водоочистительных станциях. Отметим лишь некоторые из известных работ:
М. Кейн и Глекнер изучали действие озона и хлора на цисты (плотные оболочки, образующиеся вокруг одноклеточных организмов) Endamoeba hystolica и на бактерии, сопутствующие этим культурам. Установлено, что время, необходимое для уничтожения этих организмов при остаточной концентрации озона 0.3 мг/л составляет 2-7.5 мин, а для хлора (остаточная концентрация 0.5-1 мг/л) гораздо больше – 15-20 мин.
Вирусологи США и Германии в 40х-60х годах провели ряд исследований с суспензиями вируса полиоэмилита в целях его инактивации с помощью хлора, озона и двуокиси хлора .
Выводы из этих исследований могут быть представлены в следующем виде:
Инактивация вируса полиомиелита хлором достигается дозой 0.1 мг/л при температуре воды 18 ºС, при температуре воды 7 ºС доза хлора должна быть не менее 0.25 мг/л.
Инактивация вируса с помощью озона достигается дозой 0.1 мг/л при температуре воды 18 ºС, для холодной воды 7ºС доза должна быть повышена до 0.15 мг/л.
При использовании двуокиси хлора необходимо использовать дозу 0.6 мг/л (18 ºС). Для воды с температурой 7 ºС доза двуокиси хлора должна составлять 1 мг/л.
По данным Науманна возбудители полиомиелита уничтожаются озоном за 2 мин при концентрации 0.45 мг/л, тогда как при хлорировании дозой 1 мг/л для этого требуется 3 часа.
По мнению ряда авторов, озон успешно устраняет микроводоросли и простейшие активнее, чем хлор. Так озон при концентрации 15 мг/л за 3 мин разрушает виды простейших, которые сохраняют свою активность при обработке воды дозой хлора 250 мг/л в течение продолжительного времени.
Личинки моллюска дрейсены при дозе озона 0.9-1.0 мг/л погибли на 90%, при дозе 2 мг/л – 98%, при дозе 3 мг/л – полностью. Взрослые формы моллюска погибали при более длительной обработке озонированной водой (до 30 мин).
Правда, цветущие водоросли, обычно бурно размножаются в открытых бассейнах на солнечном свете, слабо подвержены действию озона. Здесь используют ударные дозы хлора. Эту обработку проводят обычно ночью при профилактической чистке таких бассейнов.
Риденор и Инголс из США обрабатывали хлором и озоном суспензии e-coli в дистиллированной воде при Нр = 6.8 и температура 1 ºС. В этих условиях бактерицидные дозы, вызывающие гибель 99% колоний e-coli составляли для хлора 0.25-0.3 мг/л за 16 мин, а для озона 0.5 мг/л за 1 мин.
Многолетняя история использования этих двух дезинфектантов на больших водоочистных станциях содержит богатый фактический материал, позволяющий судить об их преимуществах и недостатках. В упоминавшейся уже книге «Озонирование воды» приводится ряд интересных примеров.
Так за время длительной эксплуатации станции в Ницце в озонированной воде никогда не обнаруживалось появление бактерий Escherichia coli и Clostridium pertringers.
На фильтровальной станции Бельмонт в Филадельфии (США) озонирование воды показало результаты по устранению e-coli более успешно, чем результаты достигнутые при хлорировании.
Исследования по озонированию воды проводились на Восточной водопроводной станции в г. Москва. Эффект обеззараживания воды озоном при содержании общего количества бактерий в 1 мл 800-1200 ед. составляет: при дозе озона 1 мл/л 60-65%, при дозе 2 мл/л – 85%, при дозе 3 мл/л – 90-95%. Приемлемой дозой озона следует считать 3-4 мл/л.
На Рублевской водопроводной станции (г. Москва) проводили озонирование воды реки Москвы. Общее число бактерий в 1 мл воды после введения озона снижалось на 92-99% в пределах времени от 1-25 мин. Бактерицидная доза озона соответствовала такой, после обработки, которой нельзя было обнаружить e-coli в 500 мл. воды. Повышение мутности с 6.8 до 12 мг/л и цветности с 3.2 до 18 град. требовало увеличения бактерицидной дозы озона с 3.2 до 4.1 мг/л.
Так сопоставляя работу французской станции водоподготовки в Сен-Мор и станции в Чикаго (США) В. Ф. Кожинов отмечает, что в первом случае болезни «водного происхождения» были зарегистрированы лишь в 1 случае на 100 тыс. жителей, хотя концентрация остаточного озона в воде не превышала 0.05 мг/л.
В то же время в Чикаго имели место вспышки желудочно-кишечных заболеваний несмотря на весьма значительное содержание хлора в водопроводной воде.
Один из крупнейших гигиенистов прошлого века Уотсон высказал на международном конгрессе по водоснабжению в Стокгольме (июль 1964 г.) такое мнение: «Наиболее существенным возражением против озонирования обычно считают отсутствие остаточного озона в разводящей водопроводной сети, тогда как при хлорировании в сети может быть обнаружен остаточный хлор. Эксперименты, проведенные в г. Аштоне (Англия) показали, что в обеззараженной озоном воде, циркулирующей в исправной водопроводной сети трубопроводов, не происходит ухудшение ее качеств. Контрольные пробы озонированной воды, взятые из сети, оказались совершенно равноценными пробам, содержащим остаточный хлор в воде, взятых из других источников. Установлено также, что небольшие количества остаточного хлора, имеющиеся в трубопроводах, не могут оказать никакого обеззараживающего действия на загрязнения, вызванные повреждениями коммуникаций. Т.е. присутствие остаточного хлора в трубопроводах еще не означает непременной бактериальной чистоты воды, хотя зачастую ее считают именно такой .
Один из авторов этого обзора обсуждал данную проблему с ведущими работниками цюриховского водопровода, и они подтвердили мнение Уотсона, что при использовании чистых труб в водопроводных сетях, повторного заражения озонированной воды не происходит.
Даже из этого краткого сопоставления озона с другими окислителями-дезинфектантами преимущества озона бесспорны.
Подводя некоторый итог предельно краткому сопоставлению озона, хлора и двуокиси хлора как агента для очистки и обеззараживания воды отметим, что в определенном смысле этот спор был решен самой жизнью. Действительно опыт работы водоочистительных станций, использующих озон и хлор полностью свидетельствует в пользу озона.
1.6 Другие преимущества озона.
Из-за краткости обзора мы не останавливаемся здесь на таких положительных свойствах озона как усиление процессов коагуляции-флоккуляции, эффективное воздействие на процесс микрофлоккуляции, несравненно более высокое качество воды в плавательных бассейнах, использующих озон вместо хлора и ряд других.
Наконец, проблема стоимости. Бытует мнение, что озонирование значительно дороже хлорирования. Однако это не так. В процессе хлорирования возникает необходимость устранить излишний хлор из воды, провести так называемое дехлорирование. Обычно это делают, применяя специальные реагенты. С учетом этого фактора, а также тенденций непрерывного понижения цены на озонаторное оборудование и повышение цены на хлор и хлор-продукты, в настоящее время стоимость этих процессов практически сопоставима.
Тем не менее, хлорирование, если говорить о нашей стране, используется чаще, чем озонирование. Почему? Есть несколько причин.
Работать с хлором, особенно если речь идет о баллонах с жидким хлором, сравнительно просто. Достаточно отвернуть вентиль баллона или вылить в бассейн ведро гипохлорита, как, в первом приближении, все проблемы с дезинцификацией решены. Это, безусловно, проще, чем следить за концентрацией озона, выходящего из озонатора, учитывая, что озонатор сравнительно сложный аппарат и надо быть уверенным, что он неожиданно не отключится.
Вот здесь и возникает вторая (а может быть и первая) причина слабой распространенности озона. До самого последнего времени надежность озонаторного оборудования оставляла желать лучшего, а низкий уровень автоматизации предполагал необходимость использования обслуживающего персонала относительно высокой квалификации.
В разделе «Получение озона» мы остановимся на рассмотрении этой проблемы более детально и критически рассмотрим существующие конструкции именно под углом надежности и простоты оборудования. Лишь последнее поколение озонаторов фирмы «Позитрон» позволяет за счет высокой автоматизации и надежности конструкции, свести обслуживание озонирующей аппаратуры к минимуму, точнее к нажатию одной кнопки.
1.7 Токсикология озона
Токсичные свойства озона стали предметом многочисленных исследований, начиная с 40х годов прошлого столетия. В это время в Лос-Анджелесе (США), а затем во многих других городах, наблюдалось появление так называемого фотохимического смога. Под действием солнечной радиации автомобильные выбросы (углеводороды и окись азота) трансформировались в результате сложной цепи фотохимических реакций в озон и органические перекиси, в том числе в бензопирен-очень сильный канцероген. При этом в ряде случаев концентрация озона достигала 10 ПДК (≈ 1 мг/м³). У людей, подвергшимся действию фотохимического смока, наблюдалось раздражение глаз и слизистых оболочек дыхательного тракта. После пребывания определенного времени на свежем воздухе неприятные симптомы исчезали.
Технический прогресс и в первую очередь применение каталитических нейтрализаторов автомобильных выбросов практически полностью устранили причины, вызывающие фотохимический смог. Тщательные экспериментальные исследования на людях и животных прояснили достаточно полно вопрос о токсичности озона. Можно сказать, (по нашему мнению) что в определенном смысле страхи о токсичности озона являются мифом. Да, озон относят к веществам с первым классом опасности. Его ПДК ниже, чем у таких веществ как хлор и цианистый водород (ПДК хлора = 1 мг/м³, ПДК цианистого водорода = 0.3 мг/м³). Дело в том, что при установлении величины ПДК учитывается не только летальная доза, но и упругость пара данного вещества. Так как озон крайне летучий газ (Тº кип = -111 ºС), то значение токсичности оказывается высоким. Но, необходимо подчеркнуть, что за полтора столетия знакомства человечества с озоном неизвестно ни одного случая летального отравления озоном. Да и вообще не наблюдалось ни одного случая серьезного отравления озоном, который бы потребовал пребывание в медицинском стационаре. Наибольшее влияние озон оказывает на органы дыхания. Меняется частота дыхания, объем воздуха при вдохе, жизненная и остаточная емкость легких. Но в книге венгерского специалиста по озону М. Хорвата описан эксперимент, в котором 5 человек помещали в специальную камеру с максимальной выдержкой 6 ррм озона в течение 1 часа (6 ррм ≈ 120 ПДК) и минимальной 1.2 ррм (≈ 24 ПДК) в течение 2.5 часов. Ощущение вкуса, давление крови, частоты пульса не было обнаружено. Было найдено, что снижалось ощущение запаха, однако не ясно, воздействует ли озон на нервную систему или «перебивает» запах вещества датчика. Не было обнаружено также никакого изменения в составе крови.
Опыты, проведенные на малых животных, показали, что имеется привыкание организма к озону, после чего он способен переносить и летальные дозы. Однако необходимо сделать существенное замечание именно по летальным дозам озона.
Одному из авторов этого обзора приходилось при работе с озоном, в силу непредусмотренных обстоятельств вдыхать озон в концентрации 20-40 г/м³, что соответствует (10-30)- 10³ ррм, и лежит много выше летальной кривой 4. Ощущение было весьма неприятным, но пребывание на свежем воздухе полностью восстановили нормальное дыхание. Даже если у человека насморк, и он не ощущает запах озона, сейчас в продаже имеются простые и надежные «озоновые щупы», позволяющие быстро найти любую утечку озона.
1.8 Заключение
Озон, как уникальный окислитель-дезинфектант получил широкое распространение в мире, в первую очередь в области подготовки питьевой воды. Во Франции, например, функционирует несколько тысяч водоочистных предприятий, использующих озон. Физико-химические свойства озона весьма своеобразны. Он хорошо растворяется в воде, но быстро в ней разлагается, особенно если есть примеси загрязнителей. Поэтому время жизни, особенно с нейтральным РН может меняться от часов (сверхчистая вода) до секунд (щелочные растворы, органические примеси).
Как сильный окислитель (его окислительный потенциал уступает, из стабильных веществ, только фтору), озон окисляет практически все металлы, исключая золото. Со многими веществами озон реагирует с взрывом. Озон реагирует с растворами хлора в воде, что существенно при использовании этих веществ для обработки воды в плавательных бассейнах. Реакции с органическими веществами зависят, в первую очередь, от природы органических веществ. Соединения с ненасыщенными связями окисляются очень быстро. Другие же вещества, как органические кислоты (щавелевые, уксусные, и.т.п), а также спирты и кетоны реагируют очень медленно. Скорости реакций с озоном в растворе зависят очень сильно от РН среды, т.к. в кислой среде реализуется молекулярный механизм окисления, где действует сам озон, а в щелочной – радикал ОН*.
Не менее, а может, и более ценным свойством озона является его чрезвычайно эффективная способность к устранению микрофлоры. Здесь он превосходит другие распространенные дезинфектанты (в первую очередь хлор) в 3-1000 раз, в зависимости от вида патогенной микрофлоры. Губительно действие озона и на такие микроорганизмы как грибы и водоросли, хотя в этом случае многое зависит от условий обработки.
Несмотря на эти очевидные преимущества в целом ряде производств (в первую очередь в водоподготовке) весьма часто вместо озона используют хлор и его соединения. Это связано с рядом предубеждений. Считается, что применение озона значительно дороже, чем использование хлора. В ряде квалифицированных сопоставлений стоимостных показателей озонной и хлорной очистки, когда учитывалась стоимость заключительного процесса дехлорирования, показано, что суммарные расходы практически одинаковы, а в ряде случаев, когда транспортировка химических реактивов затруднена или сильно затратна, использование озона выгоднее других окислителей-дезинфектантов.
Правда, само производство озона является технически более сложным процессом, чем получение хлора. Ранее часто имели место претензии к сложности обслуживания и надежности озонаторного оборудования. Сейчас эта ситуация изменилась в лучшую сторону. Последние разработки предлагаемые группой компаний VIRIL GROUP отличаются высокой степенью автоматизации. Для включения озонатора и его дальнейшей работы достаточно нажать одну кнопку.
Наконец существует предвзятое мнение о чрезвычайно высокой токсичности газообразного озона. Действительно, для озона существует весьма низкое значение предельно допустимой концентрации ПДК=0,1 мг/л. НО это объясняется в первую очередь его очень высокой летучестью (озон сжижается при -1110 C) Во всяком случае, за 100 лет существования озона не известно ни одного серьезного случая отравления им, не говоря уж об отравлениях с летальным исходом
1.9 Список литературы
Драгинский В.Л., Алексеева Л.П., Самойлович В.Г. «Озонирование в процессах очистки воды» М. Дели принт. 2007 г.
Инж. В.В. Караффа-Корбутть «Озонъ и его применение въ промышленности и санитарiи» Изд. «Образование» СпП. 1912 г.
В.Ф. Кожинов, И.В. Кожинов «Озонирование воды» М. Стройиздат 1973 г.
В.В. Лунин, М.П. Попович, С.Н. Ткаченко «Физическая химия озона» Изд. МГУ 1998г.
Manley Т.С., Negowski S.J. «Ozone» in Encyclopedic of chemical Technology. SecondEd. Vol 14. N.J. 1967.
Чуднов А.Ф. Реакция озона с неорганическими веществами. Труды кузбасского политехнического института. Г.Кемерово. 1979г.
HozvatsM.L. BilitzkilandHutter. Ozoneed. AkademiaKiado. Budapest.1985
Коган Б.Ф. и др. Справочник по растворимости. Т1 кн.1 м.1961
Manchot E. Kampsihulte Berichte b.40 2891.1907
Там же. B.43.750.1910
Андреев Н.И. Известия С-П политехнического института.1908. т.9 №19 стр.447
RonrebertE. DazOzone. Huttart 1916.
Крылова Л.Н. Физико-химические свойства комбинированной технологии переработки смешанных медных руд удоканского месторождения. Автореферат на соискание ученой степени кандидата технических наук. Москва 2008г.
Крылова Л.Н. и др. «Применение озона в гидрометаллургии. Материалы первой всероссийской конференции «Озон и другие экологически чистые окислители». 2005г. Москва, МГУ, стр155
Акопян С.З. и др. Кинетика окисления дисульфида озоном. Материалы второй всесоюзной конференции по озону. Москва, 1977, с.6
Бабаян Г.Г. и др. Обезмеживание электролитных шлаков меднохимического производства с помощью озона. стр.153.
Чтян Г.С. и др. Механизм процесса переработки медноэлектролитных шлаков озоном. Материалы совещания «Химия и технология редних элементов» Ереван. 1978г. С 122.
Семачев В.Ю. Семачев В.Ю. Разработка озонного способа очистки дымовых газов ТЭС. Автореферат дисстертации на соискание ученой степени кандидата технических наук. Москва 1987г.
Новоселов С.С. и др. «Озоновый метод очистки дымовых газов».Теплоэнергетика 1986г. №9.
Разумовский С.Д. Замков Д.Е. Озон и его реакции с органическими соединениями. М. 1974г.
DojbidoJ. Etol. «Образование промежуточных веществ в процессе озонирования и хлорирования» Wat. Res. 1999. 33. №4 р3111 – 3118.
При нормальных условиях озон – газообразное бесцветное вещество, обладающее резким запахом. Считается, что запах озона – это запах свежего воздуха после грозы. Это действительно так, но лишь в том случае, если его концентрация очень мала и составляет доли предельно допустимых концентраций (ПДК). Детальное описание физико-химических свойств озона рассматривается в многочисленных работах, в частности . Некоторые основные физико-химические свойства озона приведены в таблице 1.1.
1.1. Основные физико-химические свойства озона.
Растворимость озона в воде
При растворении озона в воде, его концентрация постепенно повышается и достигает предельных значений для данных условий.Растворимость озона в воде может быть выражена либо в виде так называемого коэффициента Бунзеа – β, показывающего отношение объема растворенного озона, приведенного к нормальным условиям, к объему воды (Vоз/Vв), либо в абсолютных значениях растворенного озона (г/л). При этом считается, что процесс растворения подчиняется закону Генри, согласно которому количество растворенного озона пропорционально давлению газообразного озона над раствором.Этот закон может быть записан в виде:
Cстац = β M ·Pγ, г/л
Где: Cстац - растворимость озона, г/л; β – коэффициент Бунзена; M – плотность озона = 2,14 г/л; Pγ – парциальное давление озона в рассматриваемой газовой среде.
Следует отметить, что растворимость озона гораздо выше основных атмосферных газов – азота и кислорода, но слабее таких окислителей, как хлор и двуокись хлора.Растворимость озона быстро повышается с понижением температуры воды.
Разложение озона в воде
Одновременно с растворением озона в воде происходит его разложение. При этом скорость его распада, как и обратная величина «время жизни», зависит от температуры воды и, в основном, от состава воды- в первую очередь от наличия в воде различных примесей, особенно некоторых органических соединений и ионов металлов. Эти положения хорошо иллюстрируются данными, приведенными на рисунке 1.2. 
Рисунок 1.2. . Разложение озона в различных видах воды при температуре 20 °С.
- Бидистиллят. 2. Дистиллят. 3. Вода «Из-под крана». 4. Фильтрованная вода Цюриховского озера.
Время жизни в однократно дистиллированной воде 20 минут, а в обычной воде несколько минут.
Реакция озона с неорганическими веществами.
Озон может реагировать с различными, находящимися в воде веществами по двум различным механизмам: непосредственно как озон (в молекулярной форме) и виде радикала ОН*, который возникает при распаде озона в воде. Считается, что в нейтральной воде эти 2 канала реакций распределены поровну. В кислой среде преобладает молекулярный механизм, а в щелочной – радикальный. Поскольку озон выступает в химических реакциях как окислитель, то можно судить о его окислительной способности по, так называемой, величине окислительного потенциала. Значение величин окислительных потенциалов различных веществ, являющихся окислителями, приведены в таблице 1.3.
Окислители |
Окислительный потенциал (Вольт) |
Относит. окслит. потенциал к ОК пот. хлор |
Гидроксил радикал |
||
Атомный кислород |
||
Перекись водорода |
||
Хлорноватистая кислота |
||
Диоксид хлора |
||
Из таблицы 1.3. следует, что озон является сильнейшим окислителем. Из стабильных веществ он уступает только фтору, резко превосходя хлор.Эффективность реакции озона с некоторыми неорганическими веществами можно оценить по начальным скоростям взаимодействующего с ними озона (точнее по удельным скоростям реакций, так называемым константам скоростей или их обратным величинам – временам реакций). Частично эти данные представлены на рисунке 1.3.
Реакция озона с металлами
Ионы железа и марганца быстро окисляются озоном до гидроксида железа и диоксида марганца. Перманганат также может быть образован по следующей реакции:2Mn+² +5O3+3H2O □ 2MnO4ˉ +3O2 + 6H+Параллельно с этим процессом происходит другой процесс – устранение марганца из раствора:
2Mn+² +2O3+4H2O □ 2MnO(ОН) 2↓ +2O2 + 4H+Окисление ионов оксида марганца, кобальта и никеля происходит со скоростями, которые отвечают величинам констант скоростей порядка 1 л/моль сек. Удаление этих металлов происходит в процессах флокуляции-фильтрации.Хром может быть окислен до шестивалентного хрома. Процесс этот сложный, требует особых условий. 5 6Свинец окисляется озоном PbO2 c константой скорости реакции порядка 10 -10 л/моль сек. Металлы, образующие комплексы с EDTA, такие как Pb, Ni, Cd и Mn, сначала проходят стадию разрушения комплекса, а затем окисляются. Такие реакции воспроизводят условия комплексообразования этих металлов с природными гуминовыми кислотами.
Реакция озона с органическими соединениями.
Электронная структура озона биполярна: с одной стороны – отрицательна, с другой – положительна. По этой причине озон может реагировать одновременно как электрофильно так, и нуклеофильно.Обычно в реакции прямого окисления веществ озоном в воде преобладает электрофильный механизм.Кинетика потребления растворенного озона различными органическими соединениями была изучена Hoigne и С.Д. Разумовским . Частично эти данные приведены на рисунке .Дать характеристику реакции всех основных органических веществ с озоном достаточно трудно. Рассматривая прямое воздействие озона, можно отметить некоторые общие положения: Насыщенные алкильные соединения реагируют с озоном очень медленно. Большинство хлорированных углеводородов и даже, ненасыщенные углеводороды не реагируют напрямую с озоном. В этом случае необходимо косвенное взаимодействие с озоном через радикал ОН. Бензол окисляется озоном очень медленно, а полициклические углеводороды быстрее.
Время реакции озона с фенольными соединениями составляет насколько секунд. Частично реакционная схема для фенола представлена на рисунке 1.5 . Ион фената реагирует более быстро, чем протонированный фенол. Следует отметить, что константы скорости весьма велики и близки для фенолов различного строения . Карбоксильные кислоты, кетовые кислоты и ряд подобных соединений представляют собой конечные стабильные продукты процесса окисления органических веществ озоном. Амины при нейтральных значениях рН реагируют весьма медленно с озоном, при рН › 8 реакции окисления проходят быстрее. Однако, в основном, реакции окисления аминов идут через ОН радикалы. Четвертичные амины (ароматические амины) реагируют с озоном быстрее. Спирты могут взаимодействовать с озоном, образуя в качестве промежуточных соединений гидропероксиды. При этом они окисляются до карбоксильных кислот, в то время как вторичные спирты – до кетонов. Карбоновые кислоты с озоном реагируют слабо или не реагируют вообще.
Меркаптаны окисляются с озоном до сульфоновых кислот. Бисульфиты и сульфоновые соединения являются промежуточными веществами. Аминокислоты, в состав которых входит сера (цистеин, цестин и метионин), реагируют быстро. Аминокислоты (составляющая часть белков) реагируют по электрофильному механизму. Среди пестицидов, содержащих эфиры фосфорной кислоты, наиболее известным является паратион. Озонирование этого соединения приводит к появлению параоксона, который более токсичен, чем паратион. Дальнейшее озонирование превращает параоксон в менее токсичные вещества (например, в нитрофенол, который затем окисляется до конечных продуктов – нитратов и СО2).
При обработке питьевой воды механизм прямого окисления через озон в молекулярной форме является основным. Константы скоростей большого числа органических соединений с озоном представлены в обзоре Hoigne .
- Озон, как инактиватор микрофлоры.
Как уже упоминалось выше, озон обладает мощным бактерицидным и вирулентным (инактивирующим вирусы) действием.В научной литературе (особенно популярной) часто утверждается, что озон действительно дезактивирует бактерии и вирусы сильнее, чем хлор (и это будет проиллюстрировано ниже), но к качественным оценкам этого преимущества надо относиться с определенными оговорками.Эффективность различных дезинфектантов хорошо иллюстрируется данными рисунка 2.1.

Рисунок 2.1. Скорость дезактивации патогенна Е-coli различными дезактивирующими агентами.
В настоящее время при оценке эффективности того или иного дезинфектанта используются так называемые С х Т критерий, т.е. произведение концентрации реагента на время действия. Можно сказать, что ВОЗДЕЙСТВИЕ (ИНАКТИВАЦИЯ) = Концентрация Время воздействия.В таблице 2.1. представлены для сравнения значения СхТ критерии для различных микроорганизмов – дезинфицирующих агентов.Таблица 2.1. Значение СхТ критерия для различных микроорганизмов (99% инактивации при 5-25 °С. СхТ критерий (Мб/л мин))
Вид микроорганизмов |
Озон рН:6/7 |
Свободный хлор рН:6/7 |
Хлорамин рН:8/9 |
Двуокись хлора рН:6/7 |
Полиовирусы |
||||
Ротавирусы |
||||
Гардиалямблацисты |
||||
Гардиа мюрисцисты |
||||
Криптоспоридиум |
||||
Для 90% инактивации (1 log) |
Очевидно, что озон превосходит такие дезинфектанты, как хлор, хлорамин и двуокись хлора.Для такого патогенна, как кишечная палочка (Е-coli) ,озон более эффективен, чем хлор, но ненамного. В то же время для криптоспоридиума отношение С Т критериев этих дезинфекторов приближается к 1000. Предполагается, что в принципе озону могут составить конкуренцию такие дезинфицирующие реагенты, как хлор, бром, йод, двуокись хлора и серебро.Молекулярный газообразный хлор, растворяясь в воде, распадается, производя хлористую кислоту HOCl, которая, в свою очередь, диссоциирует в воде на анион СЕО и катион Н. Степень этой диссоциации определяется кислотностью среды. Установлено, что при рН = 8 концентрация недиссоциироавшей кислоты ≈ 20%, а при рН = 7, концентрация НСlО≈80%. Так как сильным бактерицидным действием обладает именно НСlО, то при использовании хлора (даже в виде гипохлорита) необходимо поддерживать оптимальное значение рН.Йод, как дезинфектант, используется для дезинтификации в небольших системах водоподготовки и иногда в плавательных бассейнах небольшого объема. По своим дезинцифицирующим свойствам йод слабее хлора и тем более озона, но он более удобен в транспортировке.Бром, в принципе, может использовать для целей дезинцификации, однако, в присутствии других окислителей он образует балласты, производные кислоты HbrO3, которые являются весьма вредными и им соответствует низкое значение ПДК. Эта проблема – образование броматов при озонировании бром содержащих вод- является достаточно серьезной и мы остановимся на ней в разделе «Использовании озона для подготовки питьевой воды».Кроме того, в последнее время отечественная и зарубежная промышленность предлагает ряд органических веществ, обладающих сильным дезинфицирующим действием. Однако все они имеют те или иные недостатки и большого распространения до настоящего времени не нашли.- Долгое время использовался жидкий хлор из баллонов под давлением, что являлось большой проблемой с точки зрения безопасности. В настоящее время хлор получают в специальных аппаратах-хлоратах, при электролизе раствора поваренной соли или используют гипохлорит, который, растворяясь в воде, создает необходимую концентрацию свободного хлора. Надо отметить, что под термином «свободный хлор» понимают концентрацию хлорноватистой кислоты HСlO. Использование хлораторов вызывает необходимость в хранении запаса реагента, а гипохлорит при хранении разлагается и содержание свободного хлора падает.Озон производится на месте и все что нужно для его производства - это озонатор и электроэнергия.- Хлор ядовитый газ (ПДК для хлора составляет 1 мг/м³). Он впервые был использован как боевое отравляющее средство в первую мировую войну и жертвы его были многочисленны.Озон тоже относится к категории токсичных газов и его ПДК весьма низкий (0.1 мг/м³). К счастью, озон обладает чрезвычайно сильным характерным запахом и человек чувствует присутствие озона в воздухе гораздо раньше, чем его концентрация достигнет опасной величины (порог обоняния ≈ 0.1 / 0.5 ПДК). Необходимо подчеркнуть, что до настоящего времени неизвестно ни одного смертельного или даже тяжелого, требующего госпитализации, случая отравления озоном. Вопрос токсичности озона будет рассмотрен ниже отдельно.Одно из основных неприятных свойств хлора заключается в том, что при его реакции с большинством органических соединений возникает целый спектр хлорорганических производных, большинство из которых сильно ядовиты.Хлорфенолы и полихлорфенолы, особенно, так называемые диоксины, являются одними из сильнейших известных в настоящее врем органических ядов, причем действие этих токсинов заключается в разрушении иммунной системы человека. Так что, говоря о диоксинах, иногда используют термин «химический СПИД».Хлор очень легко взаимодействует с аммиаком, образуя хлорамины. Эти вещества обладают весьма слабым дезинфицирующим действием, но чрезвычайно сильно раздражают слизистые оболочки глаз и носоглотки.Хлорамины часто называют «связанным хлором». Этот связанный хлор в 5-10 раз более сильный раздражитель, чем свободный хлор.Озон также может образовывать промежуточные соединения (by products) при озонировании газовых и конденсированных сред. Теоретичеки можно допустить, что образующиеся by products более токсичны, чем озон.Эта проблема была предметом исследований многих ученых всего мира. Концентрации и состав промежуточных веществ, возникающих при озонировании, очень зависят от того, озонируется ли питьевая или сточная вода. Безусловно, в первом случае образуется гораздо меньше by products и состав их более очевиден. Все эти вопросы будут рассмотрены в соответствующих разделах обзора. Можно резюмировать достаточно совпадающие вопросы многолетних исследований следующим образом:
- В подавляющем большинстве случае промежуточные продукты окисления загрязнителей озоном МЕНЕЕ ТОКСИЧНЫ, чем исходные ингредиенты.
- Прямое сопоставление промежуточных веществ, образующихся при сравнительных экспериментах по хлорированию и озонированию, показало, что в первом случае образуется гораздо больше by products .
2.1. Дезинфекции хлором и озоном на промышленных очистных станциях и в лабораторных условиях
.
Многолетняя история использования этих 2ух дезинфектантов на больших водоочистных станциях содержит богатый фактический материал, позволяющий судить об их преимуществах и недостатках. В упоминавшейся уже книге «Озонирование воды» приводится ряд интересных примеров.Так за время длительной эксплуатации станции в Ницце в озонированной воде никогда не были обнаружены бактерии Escherichia coli и Clostridium pertringers.
На фильтровальной станции Бельмонт в Филадельфии (США) озонирование воды дало более успешные результаты по отмиранию e-coli, чем результаты, достигнутые при хлорировании.Исследования по озонированию воды проводились на Восточной водопроводной станции в г. Москва. Эффект обеззараживания воды озоном при содержании общего количества бактерий в 1 мл 800-1200 ед. составляет: при дозе озона 1 мл/л - 60-65%, при дозе 2 мл/л – 85%, при дозе 3 мл/л – 90-95%. Приемлемой дозой озона следует считать 3-4 мл/л.На Рублевской водопроводной станции (г. Москва) проводили озонирование воды реки Москвы. Общее число бактерий в 1 мл воды после введения озона снижалось на 92-99% в пределах времени от 1-25 мин. Бактерицидная доза озона соответствовала такой, после обработки, которой нельзя было обнаружить e-coli в 500 мл. воды. Повышение мутности с 6.8 до 12 мг/л и цветности с 3.2 до 18 гред. требовало увеличения бактерицидной дозы озона с 3.2 до 4.1 мг/л.Станции «Риденор» и « Инголс» из США обрабатывали хлором и озоном суспензии e-coli в дистиллированной воде при Нр = 6.8 и при температуре 1 ºС. В этих условиях бактерицидные дозы, вызывающие гибель 99% колоний e-coli , составляли для хлора 0.25-0.3 мг/л за 16 мин, а для озона 0.5 мг/л за 1 мин.Однако хлор и озон влияют на бактерии не совсем одинаковым образом. Из графика 2.3. видно, что кривая выживания бактерий падает с повышением дозы хлора, причем, идет приблизительно экспоненциальный спад числа бактерий. При озонировании наблюдается другая картина – при малых концентрациях озона его влияние на бактерии незначительно, но начиная с некоторой критической дозы (0.3-0.5 мг/л) озон резко и полностью подавляет микрофлору, в в отличие от хлора, который оставляет незначительную их часть невредимыми. Согласно некоторым исследованиям для бактерицидного действия озона необходимо определенное время. При этом озонируется вся масса бактериальных процентов. Хлор производит выборочное отравление жизненных центров бактерий, причем довольно медленное из-за необходимости длительного времени для диффузии в протоплазме.
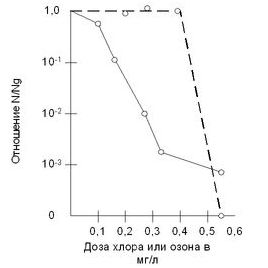
График выживания бактерий при обработке воды озоном и хлором- - - - озон-------- хлор
2.4. Действие озона на споры, цисты и другие патогенны.
По отношению к этой микрофлоре озон также выступает как эффективный бактериальный агент. В частности по Брингманну Bacillus subtilis уничтожались в воде озоном в 3000 раз быстрее, чем хлором .М. Кейн и Глекнер изучали действие озона и хлора на цисты (плотные оболочки, образующиеся вокруг одноклеточных организмов) Endamoeba hystolica и на бактерии, сопутствующие этим культурам. Установлено, что время, необходимое для уничтожения этих организмов при остаточной концентрации озона 0.3 мг/л, составляет 2-7.5 мин, а для хлора (остаточная концентрация 0.5-1 мг/л) гораздо больше – 15-20 мин.
Действие озона на вирусы
Озон оказывает ярко выраженное, радикальное воздействие на многие вирусы, что сопровождается полной гибкостью вирусного протеина. Вирусологи США и Германии в 40х-60х годах провели ряд исследований с суспензиями вируса полиоэмилита в целях его инактивации с помощью хлора, озона и двуокиси хлора . Выводы из этих исследований могут быть представлены в следующем виде:
- Инактивация вируса полиоэмилита хлором достигается дозой 0.1 мг/л при температуре воды 18 ºС, при температуре воды 7 ºС доза хлора должна быть не менее 0.25 мг/л.
- Инактивация вируса с помощью озона достигается дозой 0.1 мг/л при температуре воды 18 ºС, для холодной воды -7ºС доза должна быть повышена до 0.15 мг/л.
- При использовании двуокиси хлора необходимо использовать дозу 0.6 мг/л (18 ºС). Для воды с температурой 7 ºС доза двуокиси хлора должна составлять 1 мг/л.
По данным Науманна возбудители полиоэмилита уничтожаются озоном за 2 мин при концентрации 0.45 мг/л, тогда как при хлорировании дозой 1 мг/л для этого требуется 3 часа.
Озон и гидробионты
По мнению ряда авторов озон успешно устраняет микроводоросли и простейшие,активнее, чем хлор. Так озон при концентрации 15 мг/л за 3 мин разрушает виды простейших, которые сохраняют свою активность при обработке воды дозой хлора 250 мг/лв течение продолжительного времени. Личинки моллюска дрейсены при дозе озона 0.9-1.0 мг/л погибли на 90%, при дозе 2 мг/л – 98%, при дозе 3 мг/л – полностью. Взрослые формы моллюска погибали при более длительной обработке озонированной водой (до 30 мин). Правда, цветущие водоросли, обычно бурно размножающиеся в открытых бассейнах на солнечном свете, слабо подвержены действию озона. Здесь используют ударные дозы хлора. Эту обработку проводят обычно ночью при профилактической чистке таких бассейнов.Подводя некоторый итог предельно краткому сопоставлению озона, хлору и двуокиси хлора, как агента для очистки и обеззараживания воды, отметим, что в определенном смысле этот спор был решен самой жизнью. Действительно, опыт работы водоочистительных станций, использующих озон и хлор, полностью свидетельствует в пользу озона. Так сопоставляя работу французской станции водоподготовки в Сен-Мор и станции в Чикаго (США) В. Ф. Кожинов отмечает, что в первом случае болезни «водного происхождения» были зарегистрированы лишь в 1 случае на 100 тыс. жителей, хотя концентрация остаточного озона в воде не превышала 0.05 мг/л. В то же время в Чикаго имели место вспышки желудочно-кишечных заболеваний, несмотря на весьма значительное содержании хлора в водопроводной воде.Один из крупнейших гигиенистов прошлого века М. Т. Б. Уайтсон высказал на международном конгрессе по водоснабжению в Стокгольме (июль 1964 г.) такое мнение: «Наиболее существенным возражением против озонирования обычно считают отсутствие остаточного озона в разводящей водопроводной сети, тогда как при хлорировании в сети может быть обнаружен остаточный хлор». Эксперименты, проведенные в г. Аштоне (Англия) показали, что в обеззараженной озоном воде, циркулирующей в исправной водопроводной сети трубопроводов, не происходит ухудшения ее качества. Контрольные пробы озонированной воды, взятые из сети, оказались совершенно равноценными пробам, взятым из других источников, содержащих остаточный хлор в воде.Установлено также, что небольшое количество остаточного хлора, имеющееся в трубопроводах не может оказать никакого обеззараживающего действия на загрязнения, вызванные повреждениями коммуникаций. Т.е. присутствие остаточного хлора в трубопроводах еще не означает непременной бактериальной чистоты воды, хотя, зачастую, ее считают именно такой .Один из авторов этого обзора обсуждал данную проблему с ведущими работниками цюриховского водопровода и они подтвердили мнение М. Т. Б. Уайтсона, что при использовании чистых труб в водопроводных сетях повторного заражения озонированной воды не происходит.Даже из этого краткого сопоставления озона с другими окислителями-дезинфектантами преимущества озона бесспорны.Из-за краткости обзора мы не останавливаемся здесь на таких положительных свойствах озона, как усиление процессов коагуляции-флоккуляции, эффективное проведение процесса микрофлоккуляции, несравненно более высокое качество воды в плавательных бассейнах, использующих озон вместо хлора и ряд других. Наконец, проблема стоимости. Бытует мнение, что озонирование значительно дороже хлорирования. Однако это не так. В процессе хлорирования возникает необходимость устранить излишний хлор из воды, провести так называемое дехлорирование. Для получения воды удовлетворительного качества это приходится делать, применяя специальные реагенты. С учетом этого фактора, а также тенденций непрерывного понижения цены на озонаторное оборудование и повышение цены на хлор и хлор- продукты, в настоящее время стоимость этих процессов почти сопоставима.Тем не менее, хлорирование, если говорить о нашей стране, используется чаще, чем озонирование. Почему? Есть несколько причин: - психологическая причина. Работать с хлором, особенно если речь идет о баллонах с жидким хлором, сравнительно просто. Достаточно отвернуть вентель баллона или вылить в бассейн ведро гипохлорита, как все проблемы с дезинцификацией решены. Это, безусловно, проще, чем следить за концентрацией озона, выходящего из озонатора, учитывая, что озонатор сравнительно сложный аппарат и надо быть уверенным, что он неожиданно не отключится.- Вот здесь и возникает вторая (а может быть и первая) причина слабой распространенности озона. До самого последнего времени надежность озонаторного оборудования оставляла желать лучшего, а низкий уровень автоматизации предполагал необходимость использования обслуживающего персонала относительно высокой квалификации.Существенный прорыв в проблеме создания надежного, несложного в использовании озонаторного и озоноизмерительного оборудования стал возможен после появления современных IGBT транзисторов, позволивших резко упростить и удешевить производство импульсных высоковольтных генераторов, развитие микропроцессорной техники и новых типов ультрафиолетовых сенсоров, современных синтетических цеолитов и пр. Все это, а также полученные результаты исследований импульсных электрических разрядов в воздухе, позволило разработать новые технологические решения, открывшие совершенно новые возможности для производства озонаторов неосушенного воздуха, кислородных озонаторов, систем контроля остаточного озона в воде, озонометров
, концентраторов кислорода
и другого оборудования, делающего применение озонирования гораздо более простой и удобной технологией, чем она была раньше. Мы рады, что наши исследования и разработки, защищенные патентами в России, США, Японии и других странах помогают делать жизнь людей более простой, безопасной и,будем надеяться, более долгой.
Список литературы
Драгинский В.Л., Алексеева Л.П., Самойлович В.Г. «Озонирование в процессах очистки воды» М. Дели принт. 2007 г.
Инж. В.В. Караффа-Корбутть«Озонъ и его применение въ промышленности и санитарiи» Изд. «Образование» СпП. 1912 г.
В.Ф. Кожинов, И.В. Кожинов «Озонирование воды» М. Стройиздат 1973 г.
В.В. Лукин, М.П. Попович, С.Н. Ткаченко «Физическая химия озона» Изд. МГУ 1998г.
Manley Т.С., Negowski S.J. «Ozone» in Encyclopedic of chemical Technology. Second Ed. Vol 14. N.J. 1967.
Hozvath M.H., Bilitrki, haud., Huttez. «Ozone» Ed. Akademie. Kiado. Budapest 1987
Коган Б.Ф. и бр. «Справочник по растворимости» т.1, кн. 1, М. 1961.
Masschelein W.J. «Processes unitaixes du treatmeut de l esu potable» Ed. CEBEIOC. Hiege. 1996.
Jore M., hegube B.J. Er. Hydrol. 14.11.1983.
Cowen W.Fetal. «Chemistry in water reuse». Ed. Ann. Azboz. Science Publ. Michigan. 1985.
Curol M.D. Env. Prog. 4.46.1985.
Hoigne J. «In Progress Technologies for water treatment» Ed. Plenum. Press №3. 1988
Розумовский С.Д. и Заиков Г.З. «Озон и его реакции с органическими соединениями» М. 1974.
Hubner R. Gesundheitstechnik №12. 1973.
Dojbido J. Etol. «Образование промежуточных веществ в процессе озонирования и хлорирования» Wat. Res. 1999. 33. №4 р3111 – 3118.
Ridenour G.M., Inglols R.S. «American Jounal of Public Health» 1946. 3.6p 639.
Gomella C. 2e treitment d eux par l ozone. «Extract du mensuel» du ceutre Belge 287. 1967.
Кожинов В.Ф. Озонирование воды. «Городское хозяйство Москвы» 1970. №7.
Steinhardt. Stadtehygiene. 1S. 1956.
Naumman E. «Das gas nnd Wassertach» 1952. NY.p.81.
Dickerman J.M. etral. Journ of New England Water Works Ass. 1.11.1954.
Шалашова Е.С. «Примнение озона для чистки воды жил-ком хозяйства» №6. 1960.
Thorp C.E Jnd Med and Surg. 1950. v19 p 49
М.У. 2.1.2.694-98. «Использование ультрафиалетового измерении при обеззараживании воды плавательных бассейнов».
Г.И. Рогожкин. «Очистка и обеззараживание воды в бассейнах» Сантехника. 4.2003. стр 4-9.
Обработка воды газообразным озоном О 3 является Перспективным современным направлением в водоподготовке. Озон в силу своих высоких окислительных свойств способен эффективно уничтожать патогенную бактериальную микрофлору и окислять многие органические соединения и металлы с их последующим разложением. Озонирование воды перспективно в водоподготовке питьевой воды и воды, используемой для хозяйственных нужд, дезинфекции сточных вод, оборотной воды бассейнов, обеззараживании воды, предназначенной для бутилирования, удаляя из воды неприятные привкусы и запахи, а также для дезинфекции производственных и бытовых помещений и дезодорации воздуха. В данной статье рассмотрены основные аспекты применения озона в водоподготовке.
Очистка и получение пригодной для потребления питьевой воды является важным этапом водоподготовки. По традиционной схеме водоподготовка обычно включает три основных стадии: механическую фильтрацию, удаление из воды взвешенных и коллоидных веществ (осветление) и обеззараживание. Удаление из воды взвесей достигается при помощи сорбционных методов и фильтров. Для осветления воды применяется химическая обработка специальными коагулянтами (сернокислый алюминий Аl(SO 4) 3 ·18Н 2 О, сернокислое железо FeSO 4 ·7Н 2 О, хлорное железо FeCl 3 ·6H 2 O), способными осаждать коллоидные частицы гидроксидов железа или алюминия с адсорбированными на них коллоидами загрязнений, размером до 0,07 микрон. Для обеззараживания воды используется обработка хлором и его производными (окись хлора (ClO 2), гипохлорид натрия NaOCl), содержащими 95-97 % активного хлора. Необходимость использования трёх различных процессов существено усложняет технологию обработки воды . Из-за значительной стоимости сорбционных установок и сложности технологического процесса водоподготовки часто приходится пренебрегать улучшением вкусовых качеств воды. При обработке воды коагулянтами в воду поступают дополнительные загрязнения; хлорирование, в свою очередь приводит к образованию в воде токсически опасных хлорорганических соединений.
Альтернативным хлорированию способом в водоподготовке является обработка воды озоном. Озон – газ синего цвета с характерным резким запахом, образующийся при воздействии электрического разряда или ультрафиолетового излучения на воздух. При низких температурах (-112 °С) озон превращается в темно-синюю жидкость, при более глубоком охлаждении образует темно-фиолетовые кристаллы. T пл – 192,7 0 С, Т кип – 111,9 0 С, растворимость в воде при 20 0 С0.0394 масс.% (Табл. 1).
Таблица 1
Основные физико-химические свойства озона
Наименование параметра
Значение
Молекулярный вес
49 г/моль
Температура кипения (1 атм.)
Температура плавления (1 атм.)
Плотность (0 °С)
Растворимость в воде (20 °С)
0,0394 масс.%
Озон применяется в очистке и доочистке питьевой воды, подготовке воды для производства пива безалкогольных напитков, стерилизации стеклянных и пластиковых бутылок из полиэтилентерефталата (ПЭТ), озонирования воды в бассейнах, дезинфекционной обработке сточных вод, производственных, бытовых помещений и мест общего пользования и др.
По степени опасности озон относится к первому классу вредных веществ.
- Максимальная разовая предельно допустимая концентрация (ПДК м.р.) озона в атмосферном воздухе населённых мест 0,16 мг/м³.
- Среднесуточная предельно допустимая концентрация (ПДК с.с.) озона в атмосферном воздухе населённых мест 0,03 мг/м³.
- Предельно допустимая концентрация (ПДК) озона в воздухе рабочей зоны 0,1 мг/м³.
Химические свойства озона
По химическому строению озон представляет собой молекулу, состоящую из трех атомов кислорода с длиной связи 1.278 А 0 и валентным углом 116,8 0 (рис. 1). Молекула озона полярна, её дипольный момент 0,534 D.
Рис. 1. Химическое строение молекулы озона
Озон неустойчив и при нормальных условиях (20 0 С, 1 атм.) самопроизвольно превращается в кислород O 2 с генерированием атомарного кислорода и выделением тепла. Период полураспада озона в воздухе составляет 30-40 мин. Повышение температуры и понижение давления увеличивают скорость перехода озона О 3 в O 2 . При больших концентрациях О 3 процесс может носить взрывной характер. Контакт озона даже с малыми количествами органических веществ, некоторыми металлами или их оксидами ускоряет превращение О 3 в O 2 .
Озон - сильный окислитель и со многими непредельными органическими соединениями образует озониды – промежуточные продукты присоединения озона по двойной связи. Первичным продуктом взаимодействия озона является малозоид (1,2,3-триоксолан), который неустойчив и распадается на карбонилоксисид [>C=O-O]* и карбонильные соединения - альдегиды или кетоны (схема).
Схема. Реакция озонирования непредельных органических соединений (реакция Криге)
Реакция озонирования чрезвычайно экзотермична, избыток тепла уходит на электронноколебательное возбуждение образующихся продуктов реакции и частично рассеиваются молекулами растворителя. Промежуточные продукты, образующиеся в этой реакции, вновь реагируют в другой последовательности, образуя озониды. В присутствии веществ, способных вступать в реакцию с карбонилоксидом (спирты, кислоты), вместо озонидов образуются различные перекисные соединения.
Озон активно вступает в реакцию с ароматическими органическими соединениями, при этом реакция идет как с разрушением ароматического ядра, так и без его разрушения. При взаимодействии озона с фенолами происходит образование соединений с нарушенным ароматическим ядром (типа хиноина), а также малотоксичных производных непредельных альдегидов и кислот.
В реакциях с насыщенными углеводородами, протекающих в водных растворах, озон вначале распадается с образованием атомарного кислорода, который инициирует цепное окисление. При этом выход продуктов окисления соответствует уровням расхода озона.
Озон также способен взаимодействовать с щелочными металлами – натрием (Na), калием (K), рубидием (Rb), цезием (Cs), посредством формирования промежуточного неустойчивого комплекса катиона металла с озоном [М + – О – Н + – O 3 - ]*, в результате последующего водного гидролиза которого образуется смесь озонида МО 3 и водного гидроксида щелочного металла (MOH).
Бактерицидное действие озона
Озон – сильный дезинфектант, оказывающий выраженное бактерицидное воздействие на многие патогенные микроорганизмы, бактерии и вирусы. При оценке эффективности озона используется С·Т критерий, т. е. произведение концентрации реагента на время его действия. По своему дезинфицирующему действию озон превосходит хлор, хлорамин и двуокись хлора (Таблица 3).
Механизм бактерицидного действия озона объясняется его высокой окислительной способностью. Озон действует как сильный окислитель на клеточную стенку мембран микроорганизмов с последующим проникновением внутрь клетки и окислением жизненно важных биологически активных соединений (белки, ферменты, ДНК, РНК). Благодаряя своим окислительным свойствам озон уничтожает бактерии в 3-5 раз эффективнее УФ-излучения и в 500-1000 раз сильнее хлора.
Таблица 3
Значение С ·Т критерия для различных микроорганизмов (99% инактивации при 5-25 °С. С ·Т критерий (Мб/л ·мин))
- Вид микроорганизмов; Озон; Свободный хлор; Хлорамин; Двуокись хлора
- Кишечная палочка Е. coli; 0,02; 0,03-0,05; 95-180; 0,4-0,75
- Полиовирусы; 0,1-0,2; 1,1-2,5; 770-3470; 0,2-6,7
- Ретровирусы; 0,006-0,06; 0,01-0,05; 3810-6480; 0,2-2,1
- Гардиалямблии (цисты); 0,5-0,6; 47-150; -; -
- Гардиацисты; 1,8-2,0; 30-630; 1400; 7,2-18,5
- Криптоспоридиум; 3,2-18,4; 7200; 7200; 78
Озон более эффективен, чем хлор, при уничтожении кишечной палочки Е cherihia coli , которая в воде уничтожается озоном в 1000 раз быстрее, чем хлором. Время, необходимое для уничтожения Endamoeba hystolica при остаточной концентрации озона в воде 0.3 мг/л, составляет 2-7.5 мин, а для хлора (остаточная концентрация 0.5-1 мг/л) – 15-20 мин. Вирус полиоэмилита уничтожается озоном за 2 мин при концентрации 0.45 мг/л, тогда как при обработки воды хлором в концентрации 1 мг/л для этого требуется 3 часа.
Способы получения озона
Химический способ осуществляетсяреакцией взаимодействия пентафторида висмута (BiF 5) и других сильных окислителей с водой. Озон также образуется во многих процессах, сопровождающихся выделением атомарного кислорода, например при разложении перекисей, окислении фосфора и др.
Электролитический способ реализуется в специальных электролитических ячейках. В качестве электролитов используются растворы различных кислот и их соли (H 2 SO 4 HClO 4 NaClO 4 KclO 4). Образование озона происходит за счет разложения воды и образования атомарного кислорода, который присоединяясь к молекуле кислорода образует озон O 3 . Этот метод позволяет получать озон с высокими выходами, однако из за своей энергоемкости широкого применения не находит.
Фотохимический способ основан на диссоциации молекулы кислорода под воздействием коротковолнового УФ излучения c энергией 4.13 - 6.20 эВ. Аналогичный процесс протекает в верхних слоях атмосферы, где под воздействием солнечного излучения образуется т. н. озоновый слой. Метод нашел применение в медицине, пищевой промышленности и др.
Электросинтез в газовом разряде -барьерном, поверхностом и импульсном, получил наибольшее распространение в промышленных и бытовых установках генерирования озона. Этот метод позволяет получать озон высоких концентраций при большой производительности и невысоких энергозатратах оборудования.
Использование озона в водоподготовке
Озонирование воды в водоподготовке имет ряд неоспоримых преимуществ по сравнению с другими существующими технологиями, в т. ч. хлорированием воды (табл. 2). Важным преимуществом является неспособность озона в отличие от хлора, к реакциям замещения с органическими соединениями, приводящими к образованию побочных токсичных хлорорганических соединений – тригалометанов, главным представителем которых является хлороформ (СHCl 3). Как известно, что в процессе хлорирования воды может образовываться до 50 различных галогенсодержащих соединений, включая бромоформ (СHBr 3), дибромхлорметан (CHBr 2 Cl), бромдихлорметан (CHBrCl 2), и хлороформ (СHCl 3).
Озонирование в водоподготовке не приводит к образованию тригалометанов и за счет высокой окислительной способности озона позволяет одновременно достичь осветления воды и осаждения примесей, а также устранить привкусы и запахи при обеззараживании. По многим характеристикам, включая комплексный показатель токсичности и мутагеной активности, озон превосходит хлор и его производные (табл. 2).
Таблица 2
Сравнительные характеристики озонирования и хлорирования воды
Парамет
Хлорирование воды
Озонирование воды
Концентрация свободного остаточного реагента
не менее 0,5 мг/л
не более 0,3 мг/л
Значение рН
Мутность
До 2 мг/л
до 7 мг/л
Время контакта реагента с водой
не менее 30 минут
до 5 минут
Уничтожение Е.coli
Уничтожение вирусов
Комплексный показатель токсичности и мутагенной активности
увеличение в 3 раза
уменьшение в 2,5 раза
Органические соединения
образование тригалометанов, хлораминов, диоксинов и т.п.
разрушение органического углерода, в т.ч. хлорорганических соединений
Растворенный кислород
Уменьшение до 50%
увеличение до 100%
Ионы металлов: Fe, Mn, Al, Pb, Hg и др.
сохраняются
окисляются до 90%
При растворении в воде озон разлагается на О 2 с генерированием реакционноспособного атомарного кислорода, способного быстро окислять загрязнения органической и неорганической природы, переводя их из растворенного состояния во взвеси, задерживаемые сорбционным фильтром.
По современной технологии производство озонаосуществляется на месте потребления на специальных установках – озоногенераторах, генерирующих озон при высокочастотном коронном разряде в потоке осушенного воздуха. Расход энергии в этом процессе составляет 5–15 кВт/кг О 3 ·ч, концентрация озона в воздушно-озонной смеси - 50–250 г/м 3 . Полученный озон, затем подаётся в систему водоподготовки за барботажа и инжекции.
В крупных промышленных установках наиболее часто используется барботаж озоно-воздушной смеси через очищаемую воду . При этом, важным технологическим этапом является обеспечение одинакового времени контакта газообразного озона с водой, а также равномерное введение его по всему объему обрабатываемой воды.
В установках относительно небольшой производительности по озону наиболее распространен и достаточно эффективен метод инжекции. Очищаемая вода проходя через инжектор, создает в нем разрежение, при котором в воду поступает необходимое количество газообразного озона. Интенсивное перемешивание в инжекторе диспергирует озон на мельчайшие пузырьки с большой поверхностью контакта, что повышает скорость растворения озона в воде.
Для лучшего растворения озона в воде применяются пульсационные колонны со специальными распределительными тарелками. Озоно-воздушная смесь поступает в нижнюю часть колонны; возвратно-поступательное движение воды, создаваемое специальным пульсатором, и распределительные тарелки обеспечивают ее диспергирование до пузырьков заданных оптимальных размеров, которые поднимаются противотоком к двигающемуся вниз потоку воды. В результате этого достигается высокая степень дисперегирования озона при большой удельной производительности аппарата.
После растворения озона в воде необходимо обеспечить определенное время его контакта с водой для осуществления химических реакций окисления и удаления из воды избыточного количества непрореагировавшего озона и продуктов распада. Для этого применяется контактно-фильтровальный аппарат, из которого вода направляется на угольный фильтр на основе активированного угля для каталитического окисления продуктов взаимодействия озона с органическими соединениями с последующей их задержкой фильтром и деструкцией озона (рис. 2).
Рис. 2. Принципиальная схема озонатора воды
Применение современных передовых технологий производства озона позволяют создавать малогабаритные, надежные, высокопроизводительные и легкие в наладке и обслуживании отечественные системы озонирования воды, снабжённые датчиками электронного контроля и системами регулирования (рис. 3).
Рис. 4. Принципиальная схема системы озонирования воды. OB –осушитель воздуха; О1 – озонатор; ДУ1, ДУ2 – датчики уровня; ДО – деструктор озона; Н – насос; ОК1 – обратный клапан магистрали озона; М – манометр; И – инжектор; YA1 – электромагнитный клапан.
Выводы
Преимущества озона по сравнению с технологией хлорирования заключаются в следующих факторах:
- Озон экологически безопасен и не образует токсичных побочных продуктов распада.
- Остаточный озон быстро превращается в кислород.
- Озон вырабатывается на месте водообработки, не требуя хранения и перевозки.
- Озон уничтожает все известные микроорганизмы: вирусы, бактерии, грибы, споры, цисты, простейших и т.д. в 300-1000 раз быстрее, чем другие дезинфектанты.
- Не существует и не может возникнуть устойчивых к озону форм микробов.
- Обработка воды озоном занимает несколько минут.
- Озонирование удаляет из воды неприятные запахи и привкусы.
- Одновременно с обеззараживанием происходит осветление воды.
К недостаткам озона следует отнести сложность его производства на месте непосредственного использования, необходимость значительных энергозатрат, связанных с его получением, а также недостаточно высокую устойчивость озона в воде, разлагающегося в ней в течении 30-40 минут.
Литературные источники :
Мосин О.В . Использование озона в водоподготовке // Сантехника, 2011, ; 4, с. 47-49.
Существует два основных метода смешивания озона с водой: эжектирование и барбатирование.
Барботирование - это способ пропускания газа сквозь слой жидкости с помощью трубок, подведенных ко дну резервуара.Данная технология встречается очень часто в быту и промышленности, каждый из вас мог видеть, как насыщают кислородом воду в аквариумах, когда на дне аквариума проложены перфорированные трубки, из которых идут пузырьки воздуха, подаваемого компрессором.

При использовании метода барботажа основными характеристиками, влияющими на качество растворения озона, являются:
- Размер пузырьков (чем меньше размер, тем легче растворение)
- Внешнее давление (чем больше внешнее давление, тем лучше смешивание)
- Время прохода пузырьков через слой воды (чем дольше пузырек контактирует с водой, тем больше озона растворяется)
- Температура воды (чем ниже температура, тем лучше растворение)
Для улучшения растворимости озона при барботаже чаще всего используют три метода, а так же их комбинации:
1. Уменьшение размера пузырьков за счет уменьшения диаметра отверстий и увеличения их количества. Реализуется с помощью перфорированных трубок (барботеров) или «диффузионных камней»(«диспергаторов»).
2. Механическое перемешивание, реализуемое любым винтом или миксером, увеличивает время контакта пузырьков с водой за счет изменения направления их движения.
3. Применение «статического миксера». «Статический миксер» увеличивает эффективную толщину слоя воды за счет своей спиралевидной конструкции, тем самым увеличивая время контакта пузырьков озона с водой.

Эжектирование - данный метод позволяет проводить озонирование воды в потоке и встраивать озонатор в технологическую линию с применением высокого давления. Смешивание происходит с помощью специального устройства - эжектора (гидроструйный насос):

Смешивание методом эжектирования может применяться как с контактной емкостью (для наилучшего растворения, смешивания и увеличения времени обработки воды - применяется на линиях водоочистки, - так и без контактной емкости, выход воды сразу из эжектора, применяется для озонирования воды в потоке.
Схема очистки воды озоном в случае применения контактной емкости выглядит примерно так :
Вариант 1.

Вариант 2.
